Výpis shrnutí
Deriváty uhlovodíků
Podtémata
Deriváty uhlovodíků
Deriváty uhlovodíků jsou odvozené z uhlovodíků. Vznikají tak, že dojde k nahrazení atomu (či atomů) vodíku (\mathrm{H}) jinými atomy nebo funkčními skupinami. Některé jsou připravované uměle (třeba halogenderiváty), jiné jsou běžnou součástí živých organismů (zejména deriváty obsahující kyslík).
K dispozici jsou následující podtémata:
- Halogenderiváty a dusíkaté deriváty
- Halogenderiváty obsahují halogeny (nejčastěji \mathrm{Cl}, \mathrm{F}), příkladem je tetrafluorethen k výrobě teflonu.
- Dusíkaté deriváty zahrnují zejména aminy (primární obsahují skupinu \mathrm{–NH_2}, např. benzenamin = anilin). Nitrosloučeniny obsahují skupinu \mathrm{–NO_2}, např. 2,4,6-trinitrotoluen – TNT.
- Alkoholy, fenoly, ethery – Alkoholy a fenoly obsahují hydroxylovou skupinu (\mathrm{–OH}). Příkladem alkoholů je ethanol (líh). Ethery obsahují atom \mathrm{O} v uhlíkovém řetězci (\mathrm{–O–}).
- Aldehydy, ketony – Obsahují karbonylovou skupinu (\mathrm{C\!=\!O}). Příkladem aldehydů je methanal (formaldehyd), mezi ketony patří třeba propan-2-on (aceton).
- Karboxylové kyseliny – Obsahují karboxylovou skupinu (\mathrm{-COOH}). Příkladem je kyselina ethanová (octová) či citronová.
- Deriváty karboxylových kyselin – Vznikají buď nahrazeními na karboxylové skupině (funkční deriváty), nebo na uhlíkovém řetězci (substituční deriváty).
- Deriváty uhlovodíků: mix
Halogenderiváty a dusíkaté deriváty uhlovodíků
Deriváty uhlovodíků jsou odvozené z uhlovodíků. Vznikají tak, že dojde k nahrazení atomu (či atomů) vodíku (H) jinými atomy nebo funkčními skupinami.
Halogenderiváty
Halogenderiváty uhlovodíků ve svých molekulách obsahují atomy halogenů (\mathrm{F}, \mathrm{Cl}, \mathrm{Br} či \mathrm{I}). Živé organismy je vytvářejí jen velmi vzácně, většina je jich uměle vyrobena. Některé jsou netečné a víceméně zdravotně nezávadné, jiné jsou nebezpečné pro zdraví či dráždivé. Mnohé halogenderiváty patří mezi „věčné chemikálie“, v přírodě se prakticky nerozkládají a dlouhodobě ji znečišťují. Halogenderiváty na druhou stranu mnohdy mívají nezastupitelné a žádané vlastnosti.
Dále uvádíme příklady halogenderivátů:
- freony
- Různé komerčně vyráběné látky, které obsahují ve svých molekulách \mathrm{F} a \mathrm{Cl}.
- Dříve využívané freony (obsahující \mathrm{Cl}, např. R12 – difluordichlormethan) měly uplatnění v chladicích zařízeních a jako hnací látky do sprejů. Poškozovaly ovšem ozonovou vrstvu, od jejich používání se upustilo.
- V současnosti se v EU jako chladivo do klimatizací dopravních prostředků používá např. R-1234yf (2,3,3,3-tetrafluorpropen).
- tetrafluorethen
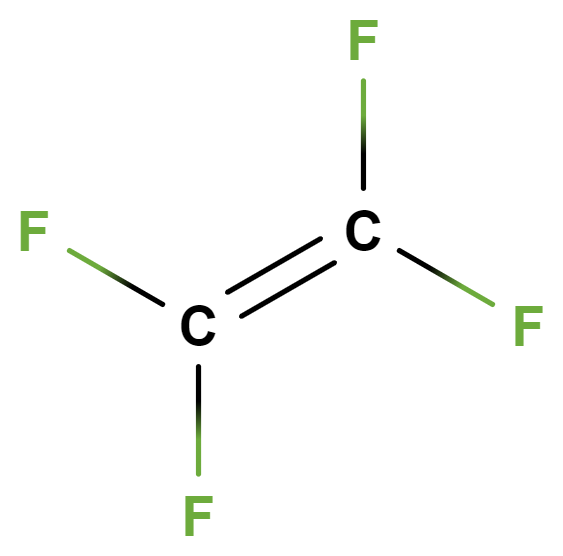
- Jeho polymerací (zřetězením molekul) vzniká polytetrafluorethen (PTFE, komerčně teflon), který se využívá např. na nepřilnavé povrchy pánví, výrobě lyžařských vosků či nepromokavých membrán do oblečení a obuvi (odpuzuje vodu). Je nehořlavý a žáruvzdorný (taje při 327 °C).
Teflon: máme se ho bát?
- Teflon sám o sobě je relativně chemicky stálý. Zdravotní riziko může plynout z jeho přehřívání (nad 260 °C), při kterém vznikají nebezpečné plyny.
- Povrch teflonových pánví se časem poškrábe, což vede k uvolňování malých částic do pokrmů.
- Při výrobě teflonu se používají další fluorované látky, které jsou toxické/nebezpečné pro zdraví. Dříve šlo o PFOA = perfluorooktanovou kyselinu, dnes jde např. látku s označením FRD-903. Teflon i doprovodné látky se v přírodě prakticky nerozkládají a předávají se v rámci potravních řetězců.
- chlorethen (vinylchlorid)
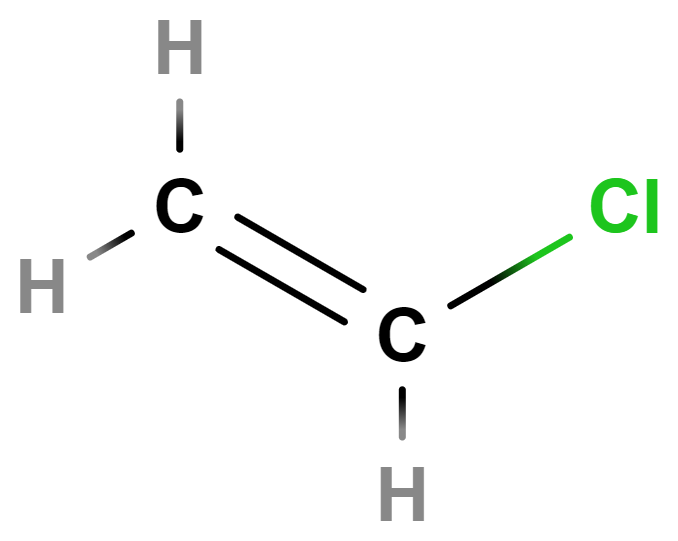
- Jeho polymerací vzniká plast PVC (polyvinylchlorid). Ten se těžko recykluje a při jeho hoření vznikají jedovaté zplodiny. Nachází nicméně využití při výrobě izolací kabelů, umělých linoleí, jednorázových rukavic či vinylových desek (gramodesek).
- tetrachlorethen (perchlorethylen)
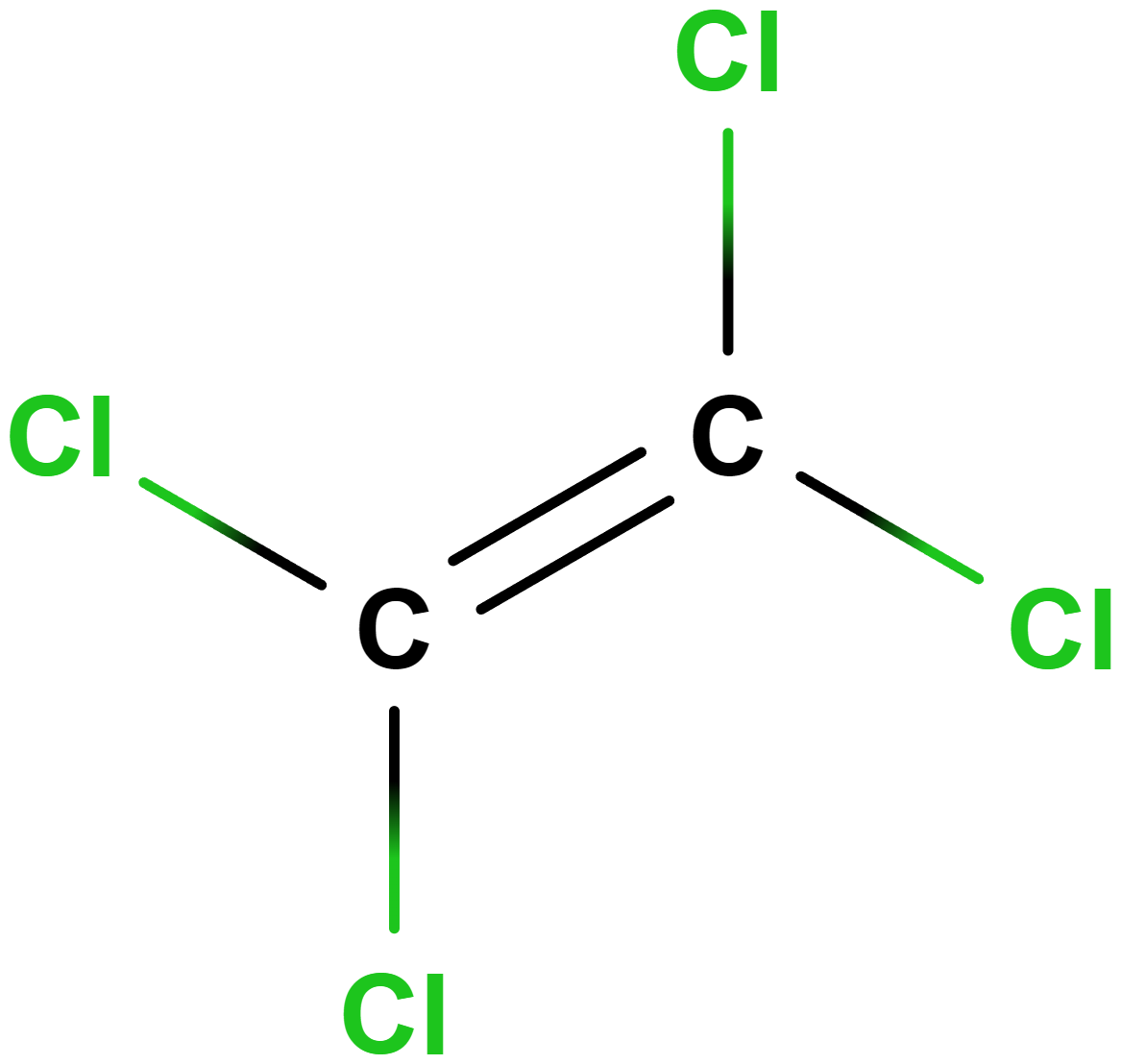
- Používá se pro suché čištění oblečení v čistírnách, dobře rozpouští tuky a další nečistoty.
- trichlormethan (chloroform)
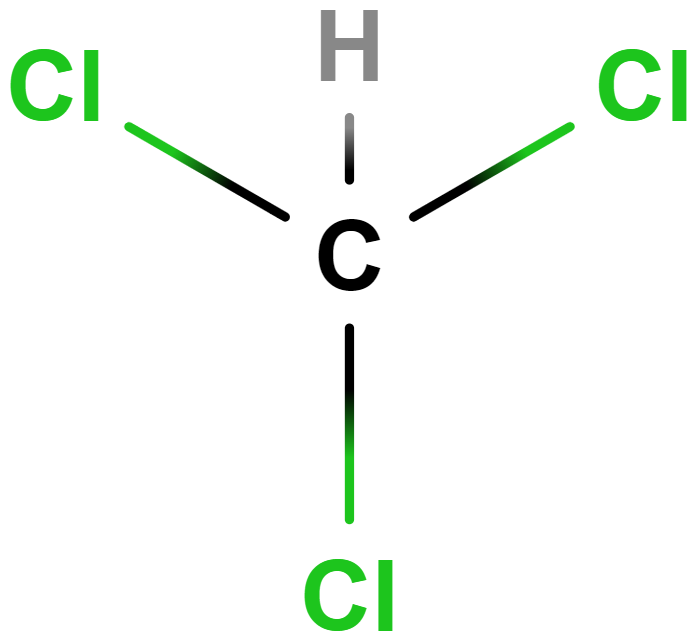
- Dříve využíván jako anestetikum, dnes v chemické syntéze nebo jako rozpouštědlo.
Dusíkaté deriváty uhlovodíků
Mezi dusíkaté deriváty uhlovodíků patří mj. aminoderiváty a nitroderiváty.
Aminoderiváty neboli aminy obsahují v molekulách skupinu \mathrm{–NH_2}. Patří mezi ně např. anilin (vzorec níže), z něhož se syntetizují barviva či léčiva.
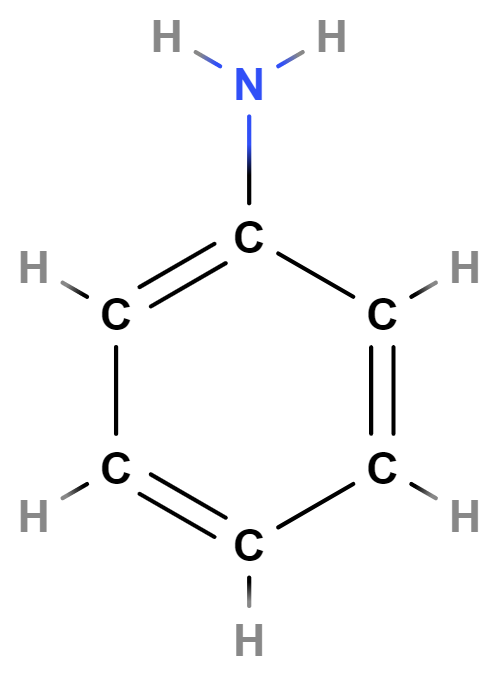
Nitroderiváty obsahují skupinu \mathrm{–NO_2}. Často se využívají k výrobě výbušnin, při jejich rozkladu vznikají obvykle \mathrm{N_2} a oxidy uhlíku v plynném skupenství. Mezi nitroderiváty patří např. TNT (trinitrotoluen) (vzorec níže) či složky trhaviny Semtex.
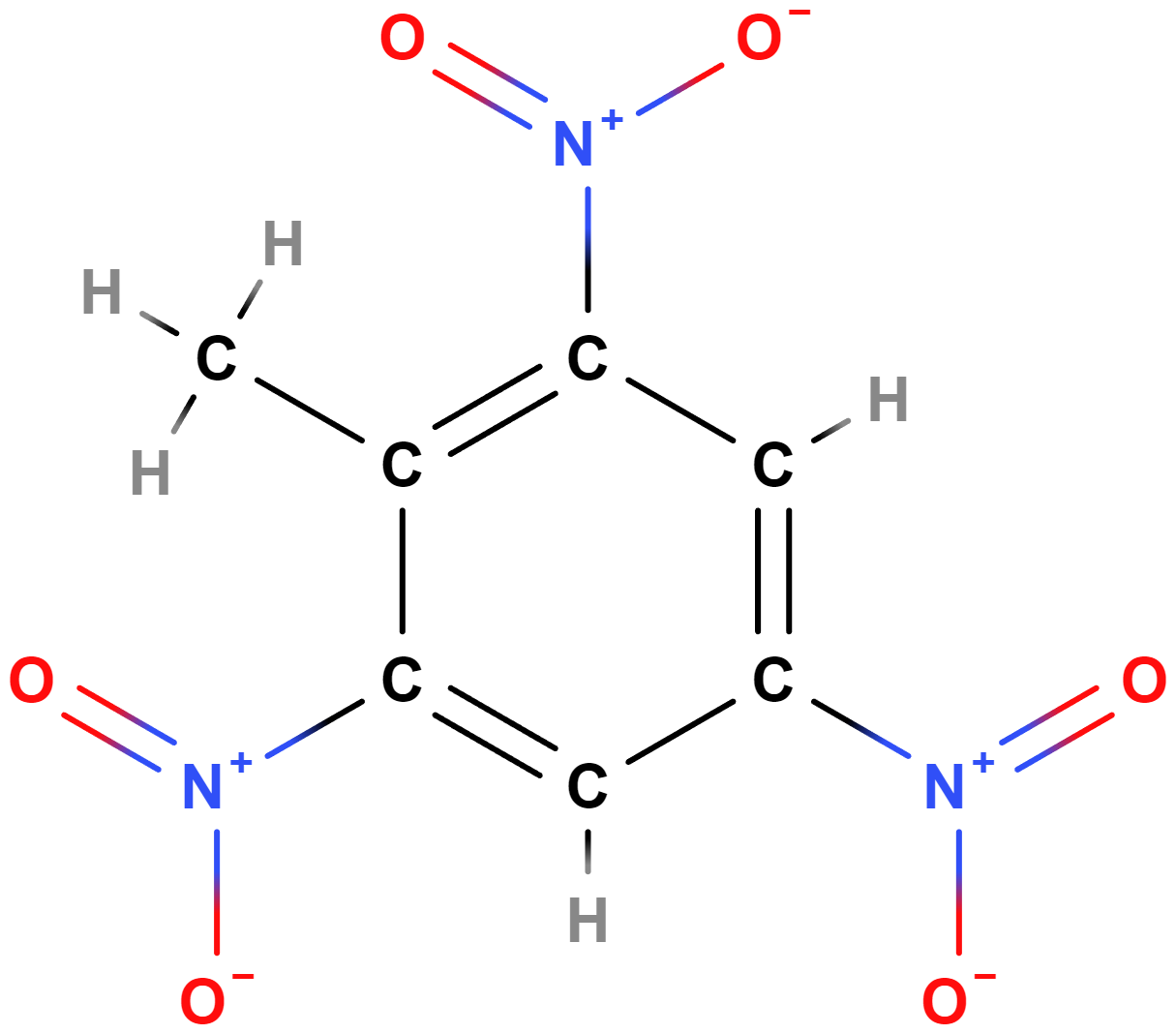
Alkoholy, fenoly, ethery
Alkoholy, fenoly i ethery patří mezi kyslíkaté deriváty uhlovodíků.
Alkoholy
Alkoholy jsou odvozené z alifatických uhlovodíků. Ve svých molekulách obsahují skupinu \mathrm{–OH}. Jejich název v základu obsahuje označení příslušného uhlovodíku s koncovkou -ol. Jde o látky běžné v přírodě, nižší alkoholy dobře mísitelné s vodou. Mezi alkoholy patří například:
- methanol
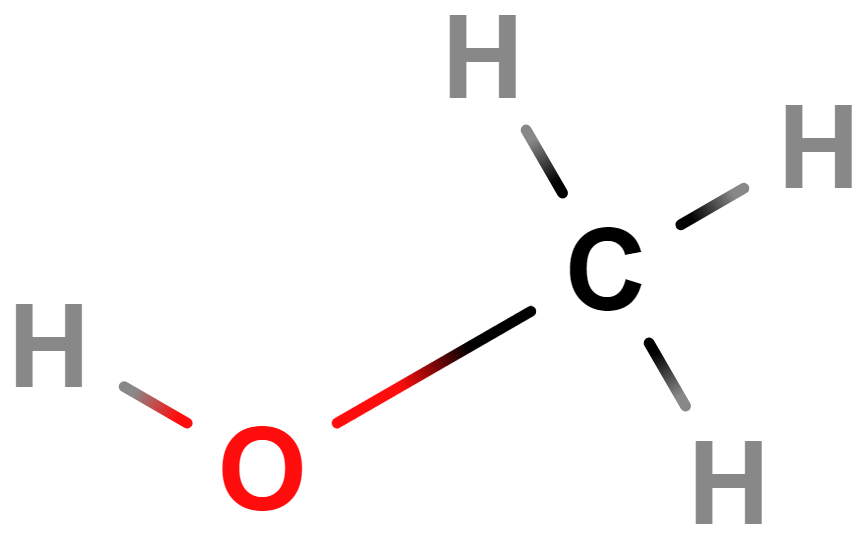
- Jedovatý, při požití hrozí oslepnutí/smrt.
- Používá se jako rozpouštědlo či k výrobě „bionafty“.
- V malém množství vzniká při kvašení, při destilaci alkoholických nápojů je nutné jej oddělit (má teplotu varu 65 °C, při zahřívání směsi se odděluje dříve než ethanol).
- V roce 2012 se v Česku odehrála methanolová aféra, kdy docházelo k ředění alkoholických nápojů methanolem. V bezprostředním časovém horizontu vedla k asi 50 úmrtím.
- ethanol (líh)
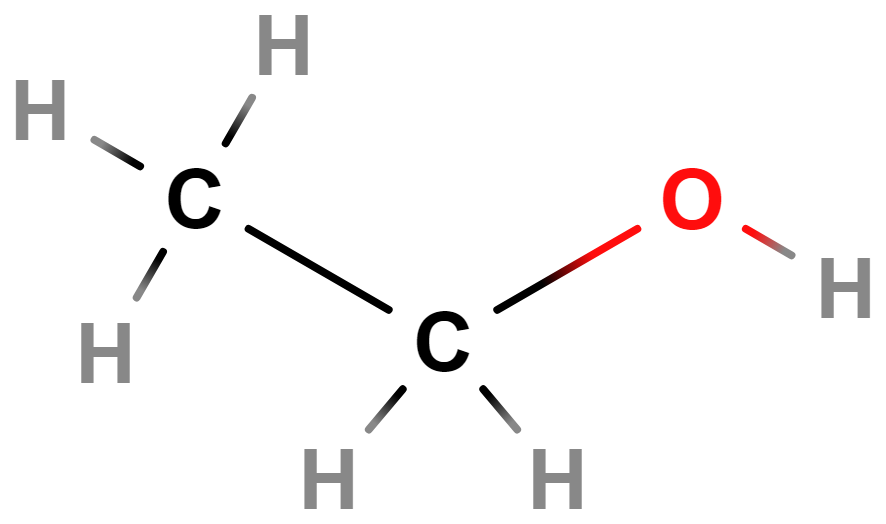
- Bezbarvá kapalina s teplotou varu 78 °C.
- Rozpouštědlo, palivo (např. do přenosných vařičů, lihových kahanů). Do lihu k technickému využití se přidávají látky, aby se nedal pít (denaturace).
- Součást alkoholických nápojů, vzniká kvašením cukrů za účasti kvasinek: \mathrm{C_6H_{12}O_6 \longrightarrow CH_3CH_2OH + CO_2}. Při požití vyřazuje z funkce určité části mozku (opilost). Pokud se mezi lidmi hovoří o „alkoholu“, myslí se tím obvykle právě ethanol.
- Játra ethanol odbourávají na toxický ethanal (acetaldehyd), který se spolu s dehydratací podílí na kocovině. Ethanal se posléze mění na kyselinu octovou, kterou lze metabolicky využít.
- Ethanol je dosud společensky tolerovanou drogou. To navzdory tomu, že jeho konzumace značně zvyšuje riziko rakoviny (nádorových onemocnění, jde o karcinogen 1. třídy) a chorob oběhového systému. Ničí játra, snadno vyvolává závislost.
- ethan-1,2-diol (ethylenglykol)
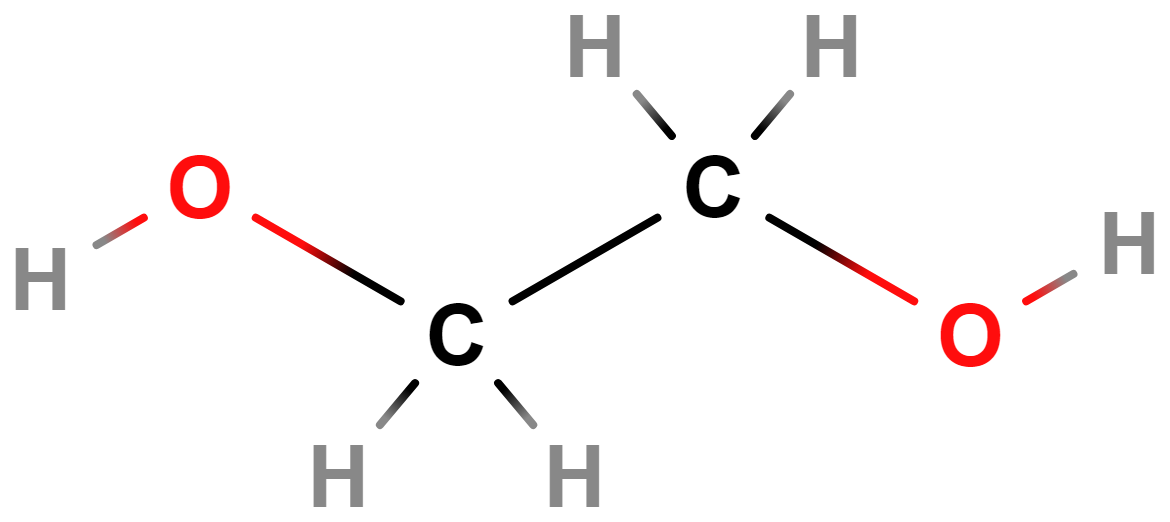
- Má teplotu tání −12,9 °C, používá se do nemrznoucích směsí či chladicích kapalin.
- propan-1,2,3-triol (glycerol)
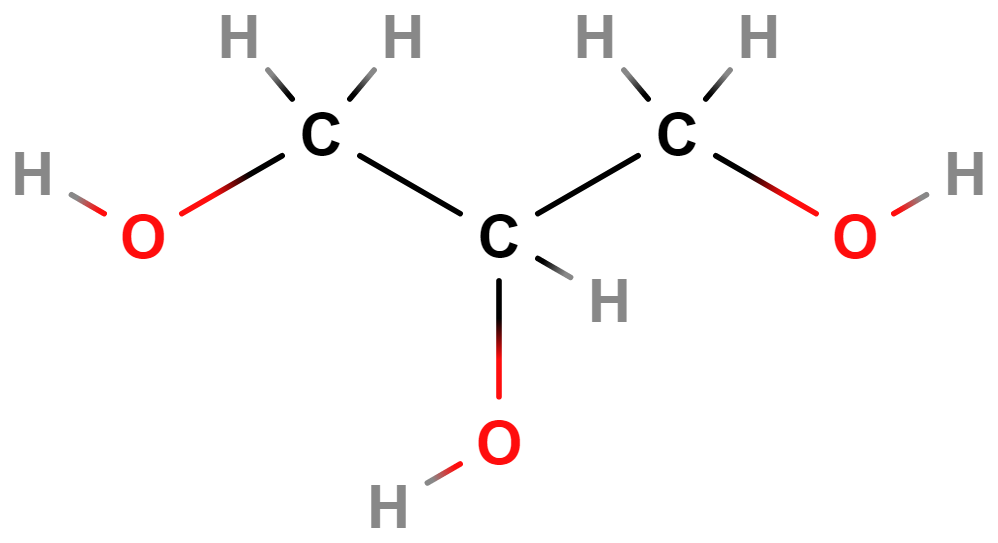
- Je součástí molekul tuků.
- Váže na sebe vodu, mnohdy se využívá v kosmetice.
Fenoly
Fenoly obdobně jako alkoholy obsahují skupinu \mathrm{–OH}, jsou však odvozené z aromatických uhlovodíků. Příkladem je fenol využívaný v chemickém průmyslu.
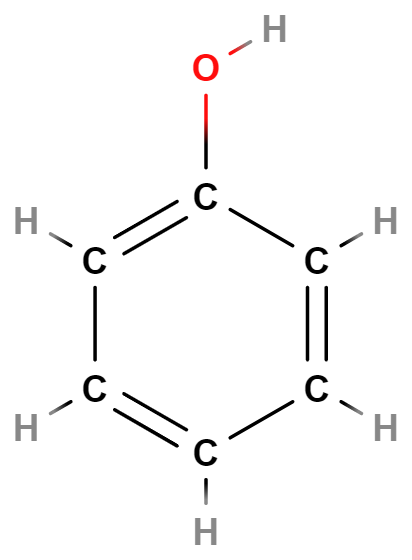
Ethery
Ve svých molekulách obsahují atom kyslíku navázaný na dva uhlovodíkové zbytky \mathrm{R–O–R'}. Příkladem je diethylether používaný jako rozpouštědlo, se vzduchem tvoří výbušné peroxidy.
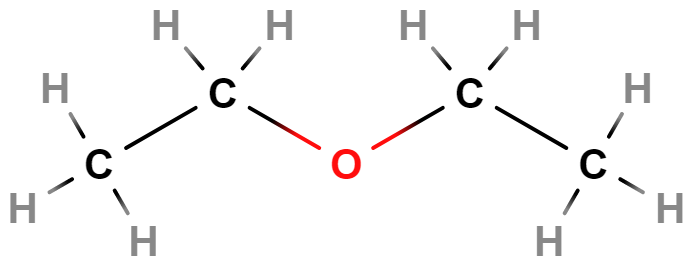
Aldehydy, ketony
Aldehydy a ketony jsou kyslíkaté deriváty uhlovodíků. Patří mezi karbonylové sloučeniny. Obsahují karbonylovou skupinu \mathrm{C\!=\!O}. Jde o látky běžné v přírodě.
Aldehydy
Aldehydy obsahují karbonylovou skupinu na konci uhlíkového řetězce. Jejich názvy mají koncovku -al. Mezi aldehydy patří například:
- methanal (formaldehyd)
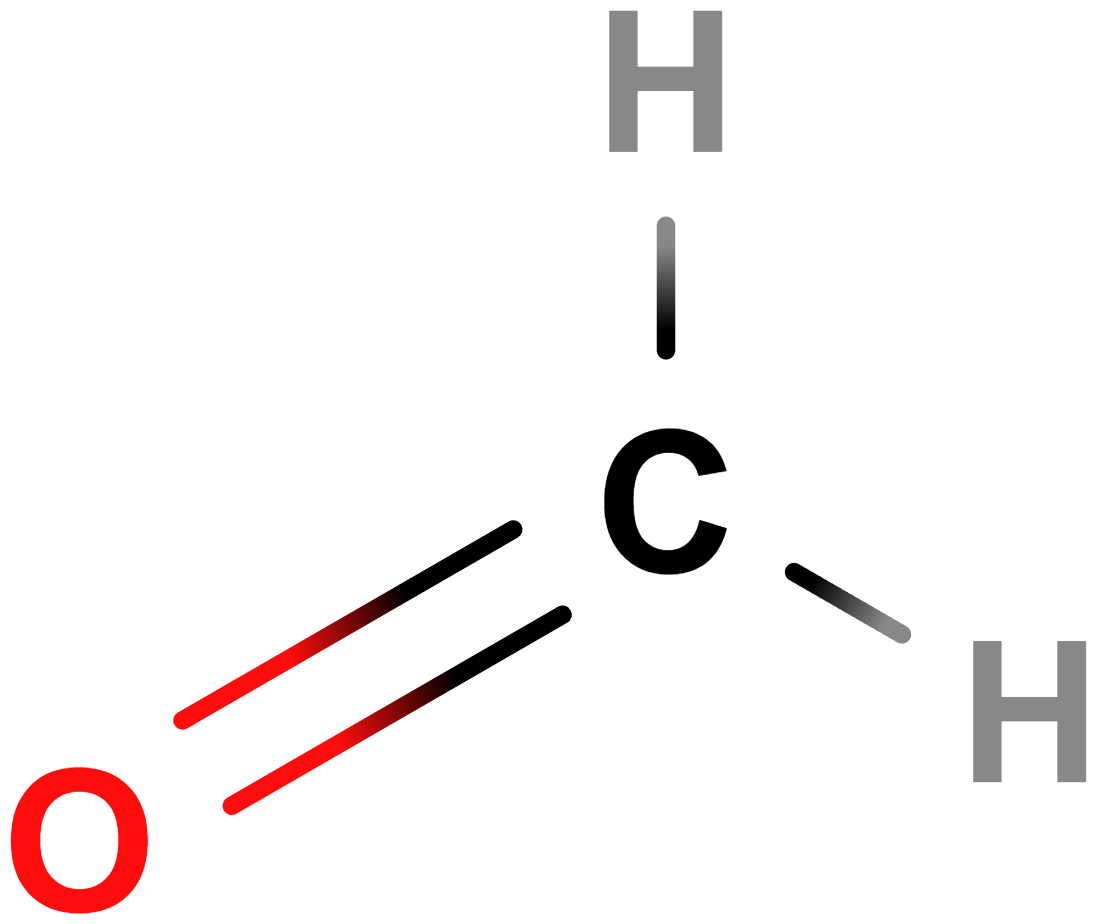
- Nejjednodušší aldehyd.
- Toxický, nebezpečný pro zdraví (karcinogenní), žíravý.
- Plyn ostrého zápachu, dobře rozpustný ve vodě. Jeho 40% roztok se označuje jako formalín, zředěný se používá ke konzervaci biologických materiálů.
- Významný pro chemický průmysl, vyrábějí se z něj různé polymery, mj. pryskyřice.
- ethanal (acetaldehyd)
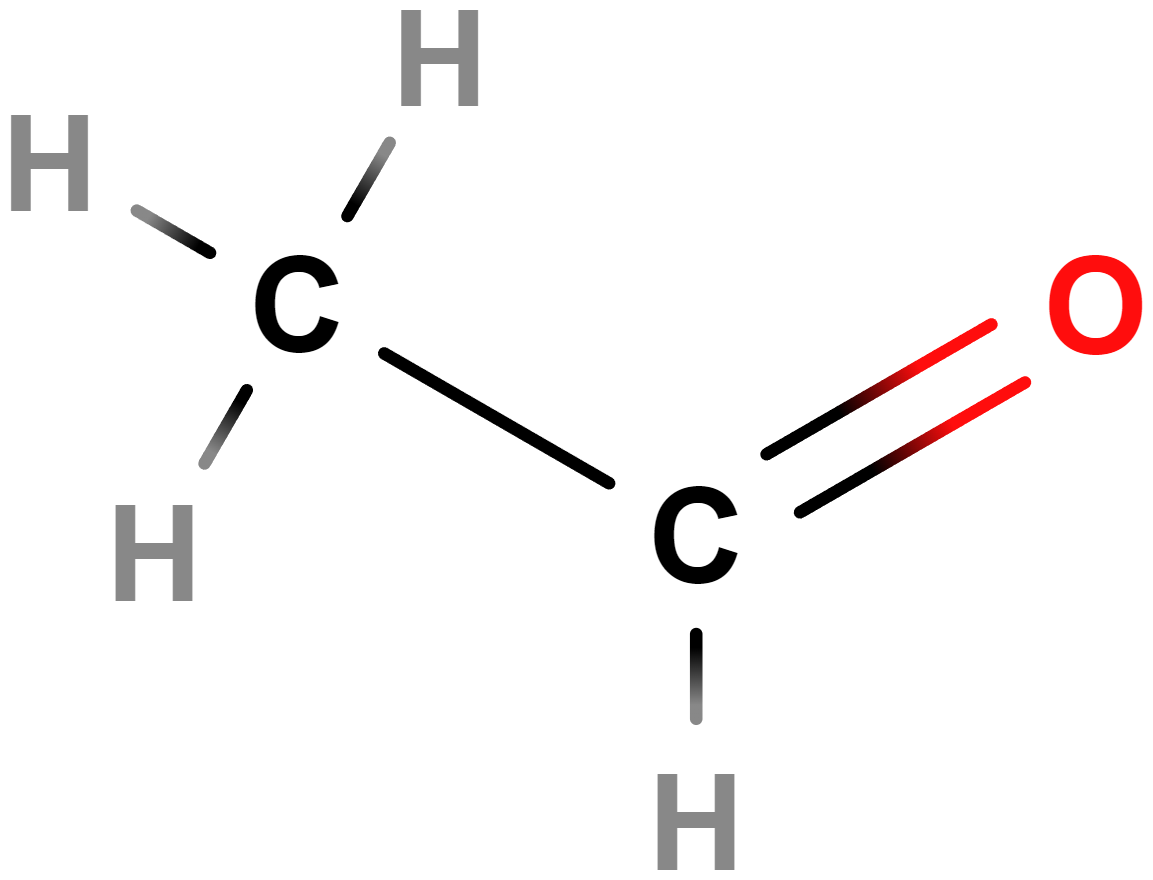
- Karcinogenní.
- Vzniká v těle při metabolických přeměnách ethanolu, podílí se na vzniku kocoviny a negativních důsledcích konzumace alkoholu.
Ketony
Ketony obsahují karbonylovou skupinu uvnitř uhlíkového řetězce. Jejich názvy mají koncovku -on.
- propan-2-on = dimethylketon (aceton)
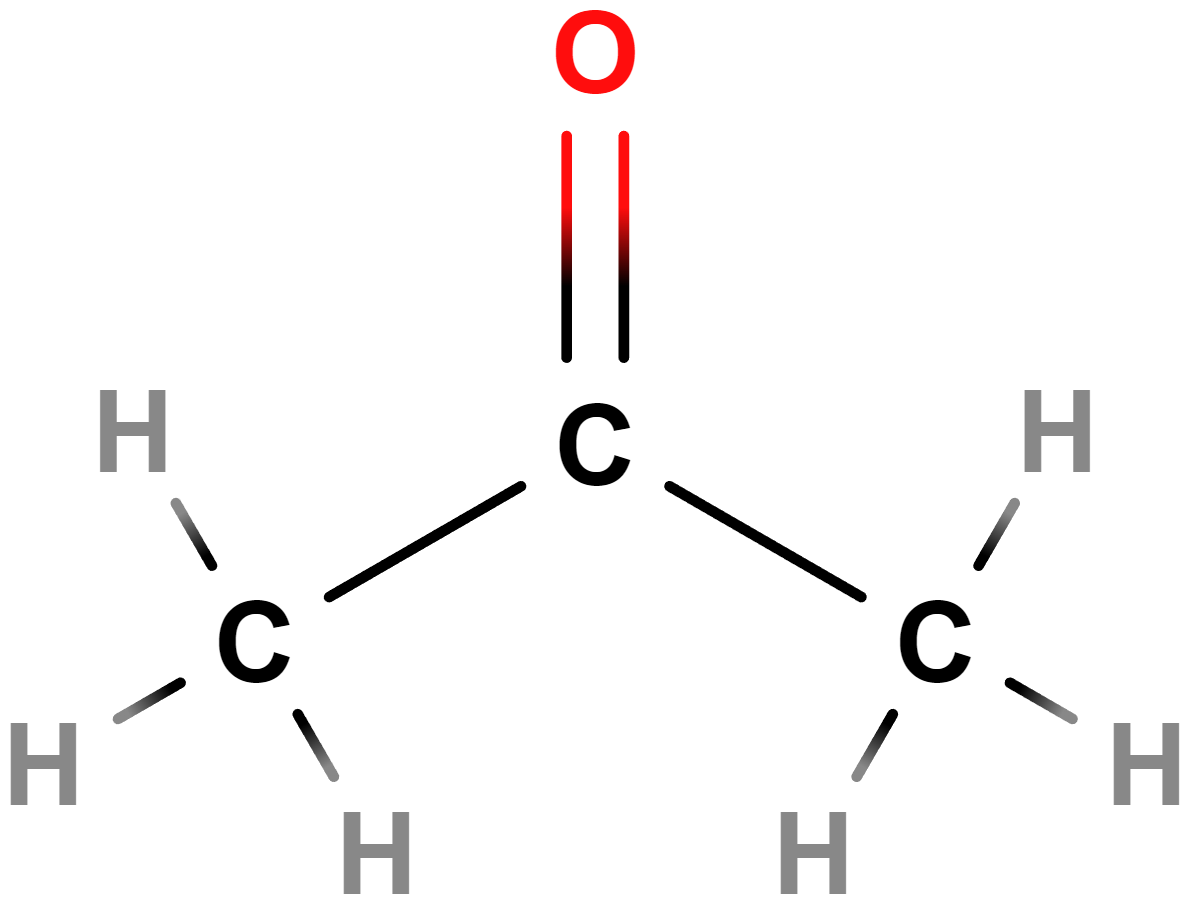
- Používá se jako rozpouštědlo.
- Hořlavý, dráždivý.
- Vzniká, když tělo nemá dostatek sacharidů (či je nemůže využívat) a pro zisk energie rozkládá tuky. Jeho přítomnost v moči (či zápach v dechu) signalizuje diabetes.
Karboxylové kyseliny
Karboxylové kyseliny patří mezi kyslíkaté deriváty uhlovodíků. Jejich molekuly obsahují karboxylovou skupinu \mathrm{–COOH}. Z této funkční skupiny se snadno uvolňuje kation vodíku (\mathrm{H^+}), což podmiňuje kyselý charakter těchto látek. Karboxylové kyseliny se běžně nacházejí v živých organismech. Karboxylové kyseliny s krátkým uhlíkovým řetězcem mají obvykle štiplavý zápach.
Příklady karboxylových kyselin
- kyselina methanová (mravenčí)
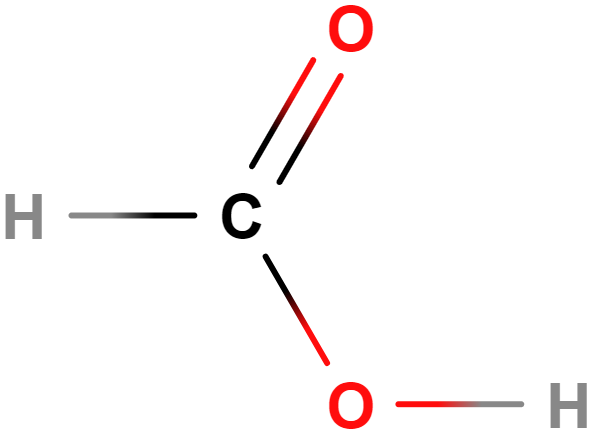
- Využívána mravenci k obraně, v žahavých chlupech kopřiv je jen v malém množství.
- Má uplatnění při hubení kleštíka včelího ve včelstvech, konzervuje rostlinnou hmotu při silážování.
- kyselina ethanová (octová)
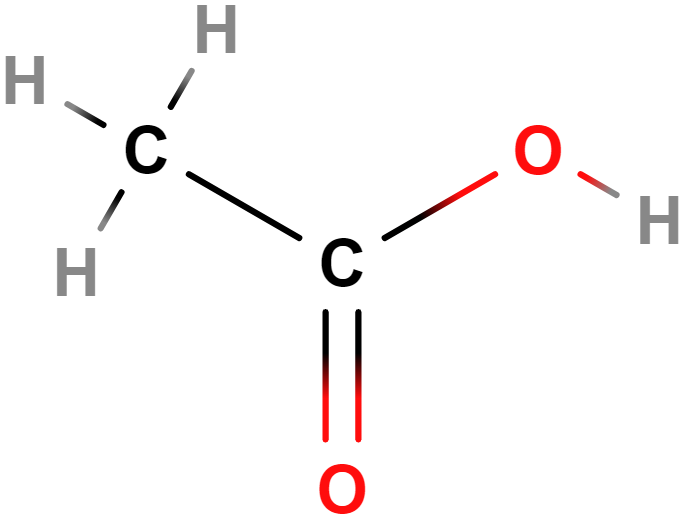
- Ocet je zpravidla 5–8% roztok. Pro potravinářské účely se vyrábí octovým kvašením ethanolu (ocet kvasný lihový, obvykle bývá uměle obarven), případně ovocných šťáv (např. jablečný ocet) či vína (balzamikový, vinný ocet).
- kyselina butanová (máselná)
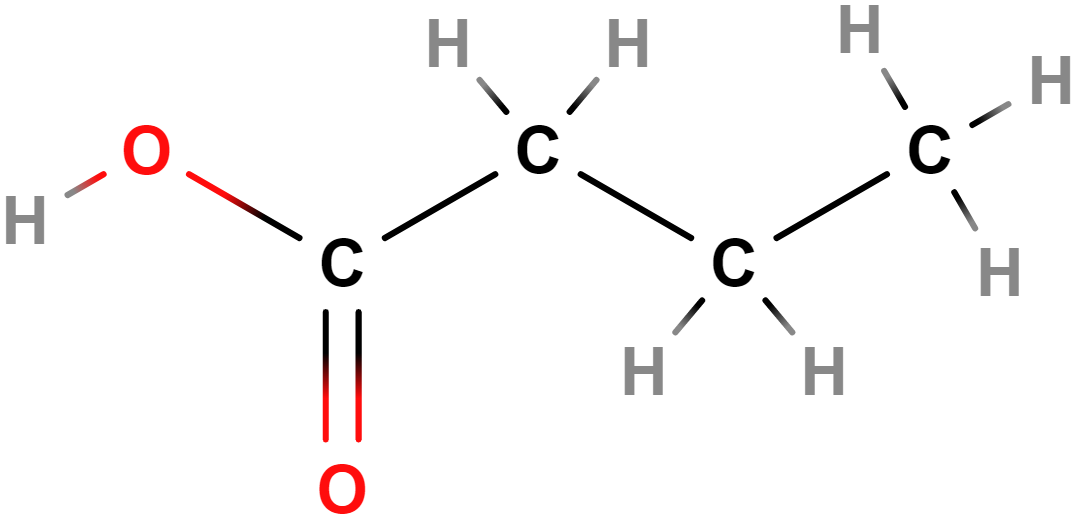
- Uvolňuje se při rozkladu tuků (např. metabolizaci tuků bakteriemi). Způsobuje např. aroma sýrů (parmezán, olomoucké tvarůžky, romadur aj.), ale také zvratků či potu.
- kyselina benzoová
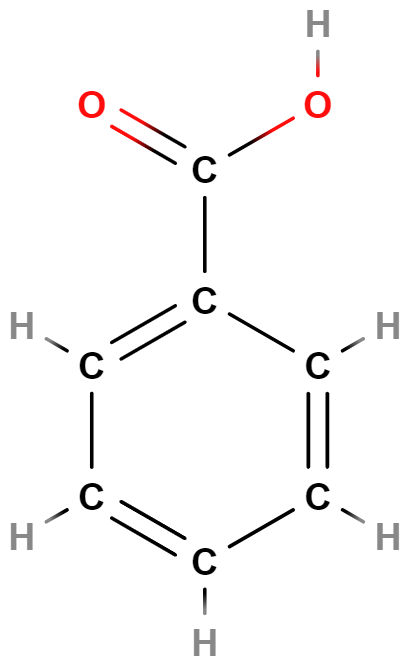
- Používá se jako konzervant.
- kyselina citronová
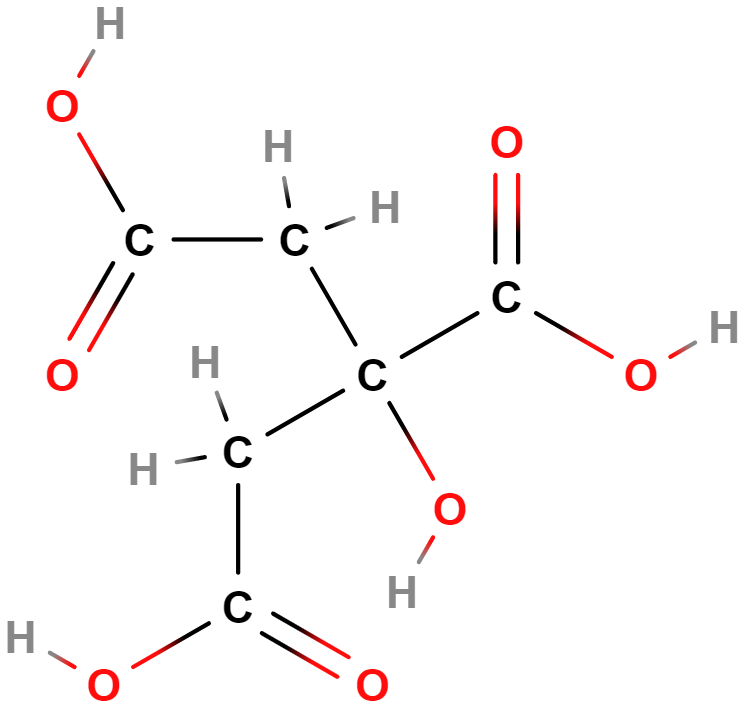
- Používá se jako konzervant či k okyselení potravin/nápojů.
- Je meziproduktem metabolismu v rámci buněčného dýchání (Krebsův cyklus = citrátový cyklus).
Mastné kyseliny tvoří součásti molekul tuků. Vyšší mastné kyseliny (např. kyselina palmitová, stearová, olejová) mají delší uhlíkové řetězce.
NahoruDeriváty karboxylových kyselin
Mezi funkční deriváty karboxylových kyselin patří např. jejich soli a estery. Funkční deriváty karboxylových kyselin vznikají vlivem zásahů do karboxylové skupiny.
Soli karboxylových kyselin
Soli karboxylových kyselin vznikají zejména jejich neutralizací. Dojde k odštěpení vodíkového kationtu (\mathrm{H^+}) z molekuly kyseliny a jeho nahrazení, nejčastěji iontem kovu. Mezi soli karboxylových kyselin patří například:
- octan sodný – Používá se proti otokům a naraženinám.
- benzoan sodný – Používá se jako konzervant.
- glutaman sodný – Jedná se o sůl aminokyseliny (kyseliny glutamové), způsobuje chuť umami.
- šťavelan vápenatý – Nerozpustná sůl, mnohdy přítomná v rostlinách (např. árónovitých). Tvoří drobné krystalky, které slouží rostlinám jako obrana před býložravci. Tato sůl je obsažena i v ledvinových kamenech.
Mýdla obsahují sodné nebo draselné soli vyšších mastných kyselin. Jejich molekuly jsou zčásti hydrofobní (odpuzují vodu, vážou se na ně nečistoty), zčásti hydrofilní (přitahují vodu, která je může i s navázanými nečistotami odplavit).
Estery karboxylových kyselin
Estery karboxylových kyselin jsou v přírodě významnými vonnými látkami (jsou např. součástí plodů, květů). Vznikají reakcí karboxylové kyseliny a alkoholu (esterifikací), produktem reakce je ester a voda. Používají se např. jako aromata do potravin, rozpouštědla či k výrobě plastů.
Ethylester kyseliny octové (ethyl-ethanoát) má využití v odlakovačích na nehty a jako rozpouštědlo. Methylestery mastných kyselin (MEŘO = methylester řepkového oleje) jsou součástí biosložky nafty. Tuky jsou přirozeně se vyskytující estery mastných kyselin a propan-1,2,3-triolu (glycerolu).
Substituční deriváty karboxylových kyselin
Substituční deriváty karboxylových kyselin mají navázané další funkční skupiny na uhlíkovém řetězci. Patří mezi ně např. hydroxyderiváty karboxylových kyselin (atomy \mathrm{H} jsou nahrazeny skupinou \mathrm{–OH}), halogenkarboxylové kyseliny (atomy \mathrm{H} jsou nahrazeny atomy halogenů) či aminokyseliny (atomy \mathrm{H} jsou nahrazeny skupinou \mathrm{–NH_2}).

