Oxidy jsou sloučeniny kyslíku s méně elektronegativními prvky. Oxidační číslo atomu kyslíku v oxidech je \mathrm{−II} (kyslík myšleně přijímá 2 elektrony od méně elektronegativního atomu).
Názvosloví oxidů
Název oxidu sestává z podstatného jména oxid a přídavného jména (obsahuje název prvku, se kterým je kyslík sloučen, s koncovkou dle jeho oxidačního čísla).
| Oxidační číslo prvku sloučeného s kyslíkem | Koncovka přídavného jména | Příklad |
|---|---|---|
| \mathrm{I} | -ný | \mathrm{\overset{\scriptsize I}{N_2} \overset{\scriptsize -II}{O}} – oxid dusný |
| \mathrm{II} | -natý | \mathrm{\overset{\scriptsize II}{C} \overset{\scriptsize -II}{O}} – oxid uhelnatý |
| \mathrm{III} | -itý | \mathrm{\overset{\scriptsize III}{Fe_2} \overset{\scriptsize -II}{O_3}} – oxid železitý |
| \mathrm{IV} | -ičitý | \mathrm{\overset{\scriptsize IV}{C} \overset{\scriptsize -II}{O_2}} – oxid uhličitý |
| \mathrm{V} | -ičný, -ečný | \mathrm{\overset{\scriptsize V}{V_2} \overset{\scriptsize -II}{O_5}} – oxid vanadičný |
| \mathrm{VI} | -ový | \mathrm{\overset{\scriptsize VI}{S} \overset{\scriptsize -II}{O_3}} – oxid sírový |
| \mathrm{VII} | -istý | \mathrm{\overset{\scriptsize VII}{Cl_2} \overset{\scriptsize -II}{O_7}} – oxid chloristý |
| \mathrm{VIII} | -ičelý | \mathrm{\overset{\scriptsize VIII}{Os} \overset{\scriptsize -II}{O_4}} – oxid osmičelý |
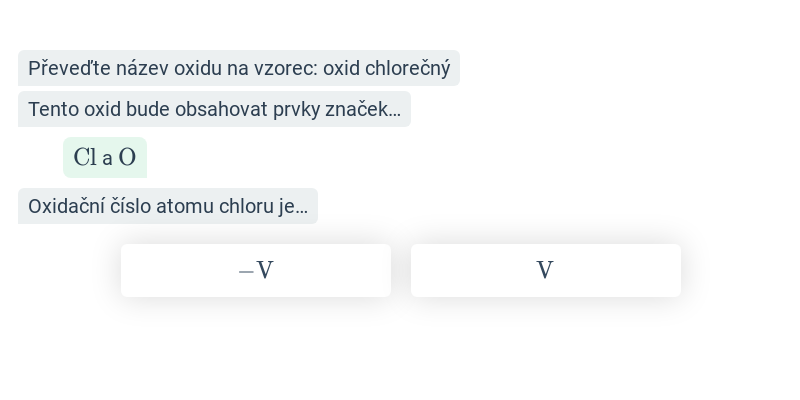
Převádění názvu na vzorec
Příklad: oxid selenový.
- Napsat značky prvků. Oxidy vždy obsahují kyslík (\mathrm{O}), který se ve vzorci píše doprava. – \mathrm{SeO}
- Kyslík má oxidační číslo −II. – \mathrm{Se \overset{\scriptsize -II}{O}}
- Oxidační číslo druhého prvku vychází z koncovky přídavného jména: selenový → selen bude mít oxidační číslo VI. – \mathrm{\overset{\scriptsize VI}{Se} \overset{\scriptsize -II}{O}}
- Součet oxidačních čísel v molekule musí být roven 0, je nutné upravit počet jednotlivých atomů.
- Pomocí křížového pravidla: oxidační číslo „převést“ na počet částic druhého prvku (\mathrm{\overset{\scriptsize VI}{Se_2} \overset{\scriptsize -II}{O_6}}) a následně vzorec zjednodušit (\mathrm{\overset{\scriptsize VI}{Se} \overset{\scriptsize -II}{O_3}}).
- Úvahou/sestavením rovnice. Selen má oxidační číslo \mathrm{VI}. Kolik v molekule musí být atomů kyslíku (s ox. č. −II), aby „vyrovnaly“ oxidační číslo \mathrm{VI}? Neboli: \mathrm{-II} \cdot x + \mathrm{VI} = 0, x = 3. V molekule musejí být 3 atomy kyslíku: \mathrm{\overset{\scriptsize VI}{Se} \overset{\scriptsize -II}{O_3}}.
- Oxidační čísla se obvykle zapisují jen jako pomůcka při tvoření vzorce, tedy výsledný vzorec by byl \mathrm{SeO_3}.
Tento postup přibližuje cvičení krok po kroku (název na vzorec).
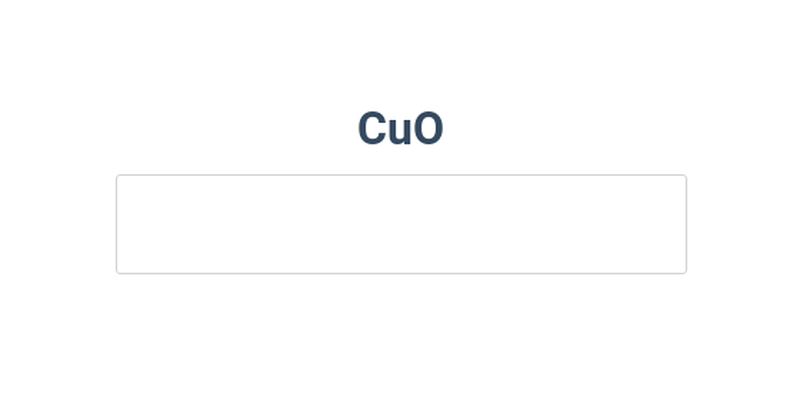
Převádění vzorce na název
Příklad: \mathrm{Al_2O_3}.
- Uvědomit si, že jde o oxid.
- Zjistit název prvku sloučeného s kyslíkem (v tomto případě jde o \mathrm{Al} = hliník). – oxid hlin…
- Zjistit oxidační číslo druhého prvku. Součet oxidačních čísel v molekule je 0.
- Každý atom kyslíku má oxidační číslo \mathrm{-II}, jsou přítomny 3 atomy kyslíku. Součet oxidačních čísel u atomů \mathrm{O} je tedy −6.
- Jsou přítomny 2 atomy hliníku (\mathrm{Al}). Jaké musí být oxidační číslo každého z nich, aby došlo k „vyrovnání“ −6 u atomů \mathrm{O}? Neboli: 2 \cdot x -6 = 0, x = 3. Oxidační číslo hliníku (\mathrm{Al}) je \mathrm{III}.
- Zjistit, jaké koncovce odpovídá dané oxidační číslo. V tomto případě \mathrm{III} → -itý, jedná se o oxid hlinitý.
Tento postup přibližuje cvičení krok po kroku (vzorec na název).
Příklady oxidů
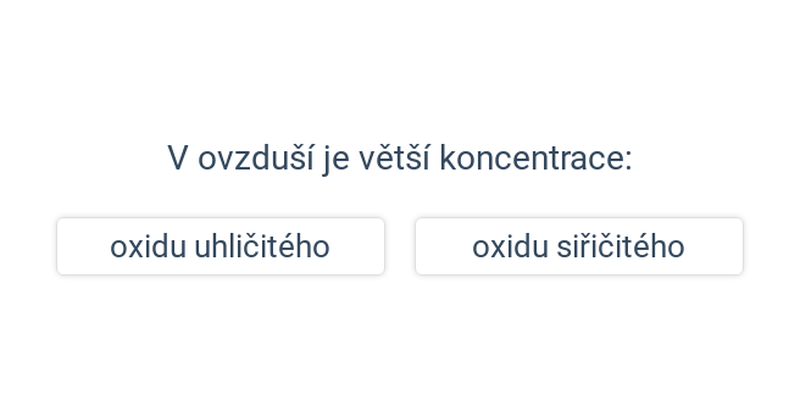
- oxid uhličitý (\mathrm{\overset{\scriptsize IV}{C} \overset{\scriptsize -II}{O_2}}) – Je potřeba pro fotosyntézu. Vzniká při buněčném dýchání (vyšší koncentrace v zadýchané místnosti negativně ovlivňuje soustředění), ale také při spalování organických látek/fosilních paliv. Ve vzduchu je ho asi 0,043 % (427 ppm). Jeho obsah ve vzduchu vlivem lidské činnosti stoupá, což prohlubuje skleníkový efekt.
- oxid uhelnatý (\mathrm{\overset{\scriptsize II}{C} \overset{\scriptsize -II}{O}}) – Vzniká při hoření za nedostatku kyslíku. Váže se na hemoglobin (červené krevní barvivo) ochotněji než kyslík, čímž zabraňuje přenosu kyslíku v těle (to je podstata jeho jedovatosti).
- oxid dusný (\mathrm{\overset{\scriptsize I}{N_2} \overset{\scriptsize -II}{O}}) – „Rajský plyn“, používá se ke znecitlivění ve stomatologii či k přípravě šlehačky.
- další oxidy dusíku – Souhrnně označované jako \mathrm{NO}_x. Jedovaté, vznikají při provozu spalovacích motorů. Jejich přítomnost vede ke vzniku přízemního ozonu.
- oxid křemičitý (\mathrm{\overset{\scriptsize IV}{Si} \overset{\scriptsize -II}{O_2}}) – Tvoří minerál křemen, je součástí mnohých hornin (např. žuly). Potřeba pro výrobu skla (ve formě sklářského písku). Jeho pórovitá forma, silikagel, se používá k pohlcování vlhkosti (typicky v malých sáčcích u různých výrobků).
- oxid titaničitý (\mathrm{\overset{\scriptsize IV}{Ti} \overset{\scriptsize -II}{O_2}}) – Využíván jako bílé barvivo, např. do temper či zubních past.
- oxid siřičitý (\mathrm{\overset{\scriptsize IV}{S} \overset{\scriptsize -II}{O_2}}) – Jedovatý. Vzniká při spalování paliv obsahujících síru (např. hnědého uhlí). Dříve způsoboval kyselé deště, nyní se zachytává při odsiřování spalin. V nízkých koncentracích se používá jako konzervant (např. u sušeného ovoce).
- oxid sírový (\mathrm{\overset{\scriptsize VI}{S} \overset{\scriptsize -II}{O_3}}) – Jeho reakcí s vodou vzniká kyselina sírová.
- oxid železitý (\mathrm{\overset{\scriptsize III}{Fe_2} \overset{\scriptsize -II}{O_3}}) – Součástí minerálu hematitu, ruda železa.
- oxid vápenatý (\mathrm{\overset{\scriptsize II}{Ca} \overset{\scriptsize -II}{O}}) – Pálené vápno, součást cementu. Vzniká pálením vápence.
Krok po kroku
Doplňování jednotlivých kroků v rozsáhlejším postupu.
Poznávačka
Procvičování pojmů nebo názvů. Obsahuje dynamickou nápovědu.
Doplňování textu
Krátké texty, do kterých doplňujete na vybraná místa správnou variantu ze dvou možností.